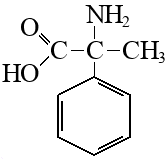
Что это такое
Фенилаланин (α-амино-β-фенилпропионовая кислота, сокращенно: Фен, Phe, F) является ароматической α-аминокислотой. Он существует в двух оптических изомерных формах — L и D, а также в виде рацемата (DL). С химической точки зрения, эту аминокислоту можно рассматривать как аланин, в котором один из атомов водорода заменен на фенильную группу.Фенилаланин структурная формула
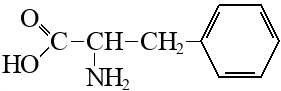
Молекула
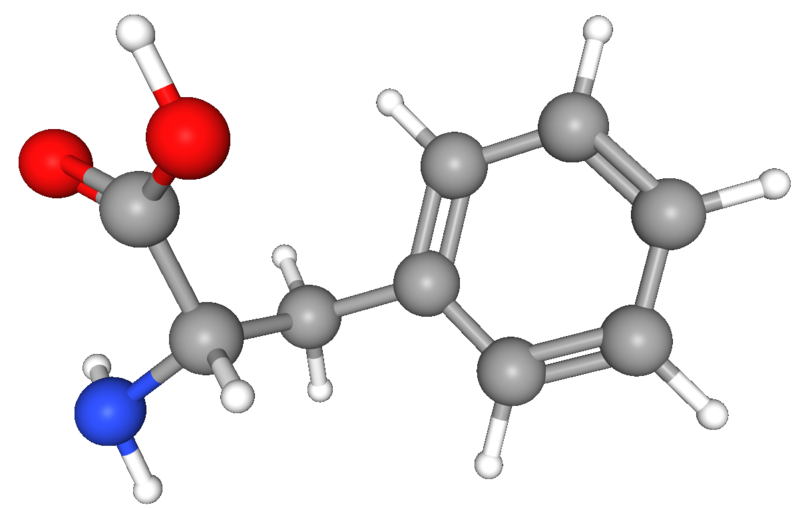
Общие, физические, термические, химические свойства
Классификация
| Систематическое наименование | 2-амино-3-фенилпропановая кислота |
| Сокращения | Фен, Phe, F, UUU, UUC |
| Химическая формула (Брутто-формула) | C9H11NO2 |
| Молярная масса | 165,19 г/моль |
| Плотность | 1,29 г/см³ |
| Температура плавления | 283 °C |
| Константа диссоциации | 2,20 |
| Изоэлектрическая точка | 5,48 |
| Константа диссоциации кислоты Ka | 2,20 9,09 |
| Рег. номер CAS | [63-91-2] |
| PubChem | 6140 и 6925665 |
| Рег. номер EINECS | 200-568-1 |
| ChEBI | 17295 и 58095 |
| ChemSpider | 5910 |
Аминокислота
Фенилаланин представляет собой протеиногенную аминокислоту, которая присутствует в составе белков у всех известных живых существ. Благодаря участию в гидрофобных взаимодействиях и взаимодействии стекинга, он играет важную роль в сворачивании и стабилизации белковых структур, являясь неотъемлемой частью их функциональных центров.Источник в продуктах
| Продукт | Содержание фенилаланина г/100г |
|---|---|
| Куриное яйцо | 7.3 |
| Картофель | 6.4 |
| Женское молоко | 5.9 |
| Коровье молоко | 5.7 |
| Соевые бобы | 5.0 |
| Рыба | 4.8 |
| Пшеничная мука | 4.8 |
| Овсяные хлопья | 4.6 |
| Мясо | 4.5 |
Образование
Фенилаланин постоянно вырабатывается в организме в процессе распада белков, поступающих с пищей и содержащихся в тканях. В природных условиях фенилаланин синтезируют микроорганизмы, грибы и растения. Фенилаланин производится в промышленных объемах методом микробиологического синтеза. Возможно также получение этой аминокислоты путем химического синтеза (например, через синтез Эрленмейера из бензальдегида или синтез Штрекера из фенилацетальдегида), после которого рацемат разделяют ферментативным способом. Фенилаланин используют для обогащения кормов для животных, в качестве ингредиента спортивных добавок и пищевых продуктов. Большая часть производимого фенилаланина идет на создание дипептида аспартама — искусственного подсластителя, который широко применяется в пищевой индустрии, особенно в производстве жевательных резинок и газированных напитков.l фенилаланин
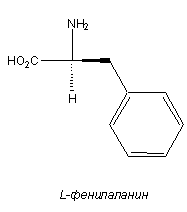 L-фенилаланин является гликокетогенной аминокислотой (аминокислота смешанного типа). Эта протеиногенная аминокислота кодируется триплетами UUU и UUC. Она входит в состав белков (встречаемость 3,78%), нейропептидов, пептидных гормонов и служит предшественником множества биологически активных соединений. Фенилаланин — незаменимая для человека аминокислота, которую необходимо получать с пищей в достаточном количестве. Рекомендованная Всемирной организацией здравоохранения норма потребления L-фенилаланина для человека составляет 25 мг на 1 кг массы тела.
Основной способ получения L-фенилаланина — это микробиологическая ферментация. Химико-ферментативным методом синтеза можно производить L-фенилаланин из коричной кислоты с использованием фермента фенилаланинаммиаклиазы (КФ 4.3.1.24).
Также возможен химический синтез фенилаланина из бензальдегида, глицина и уксусного ангидрида.
Бактерии и растения могут синтезировать L-фенилаланин из хоризмата. Биохимическим предшественником при биосинтезе L-фенилаланина у растений также может выступать фенилпируват.
Конечный продукт катаболизма L-фенилаланина — это ацилированное производное кофермента А. Генетические нарушения ферментов, участвующих в этом процессе, могут привести к наследственным заболеваниям у людей. Например, на начальном этапе катаболизма фенилаланин подвергается гидроксилированию, в результате чего образуется L-тирозин. Если этот процесс нарушается из-за дефицита фермента фенилаланингидроксилазы (КФ 1.14.16.1), то развивается фенилкетонурия.
Полученный из фенилаланина L-тирозин служит предшественником для синтеза дофамина, меланинов, адреналина и норадреналина. В растениях L-фенилаланин является предшественником многих биологически активных веществ, включая лигнин и коричную кислоту.
L-фенилаланин содержится практически во всех белках (за исключением протаминов) — около 7,8% в сывороточном альбумине, 4,6% в гамма-глобулине, 7,7% в овальбумине. Он также входит в состав пептидных гормонов (таких как соматостатин) и опиоидных пептидов (например, энкефалинов), и обнаруживается в организмах в свободной форме. Остатки D-фенилаланина являются компонентом пептидных антибиотиков (например, грамицидина S, полимиксинов, тироцидинов), нейропептидов моллюсков и ракообразных.
L-фенилаланин является гликокетогенной аминокислотой (аминокислота смешанного типа). Эта протеиногенная аминокислота кодируется триплетами UUU и UUC. Она входит в состав белков (встречаемость 3,78%), нейропептидов, пептидных гормонов и служит предшественником множества биологически активных соединений. Фенилаланин — незаменимая для человека аминокислота, которую необходимо получать с пищей в достаточном количестве. Рекомендованная Всемирной организацией здравоохранения норма потребления L-фенилаланина для человека составляет 25 мг на 1 кг массы тела.
Основной способ получения L-фенилаланина — это микробиологическая ферментация. Химико-ферментативным методом синтеза можно производить L-фенилаланин из коричной кислоты с использованием фермента фенилаланинаммиаклиазы (КФ 4.3.1.24).
Также возможен химический синтез фенилаланина из бензальдегида, глицина и уксусного ангидрида.
Бактерии и растения могут синтезировать L-фенилаланин из хоризмата. Биохимическим предшественником при биосинтезе L-фенилаланина у растений также может выступать фенилпируват.
Конечный продукт катаболизма L-фенилаланина — это ацилированное производное кофермента А. Генетические нарушения ферментов, участвующих в этом процессе, могут привести к наследственным заболеваниям у людей. Например, на начальном этапе катаболизма фенилаланин подвергается гидроксилированию, в результате чего образуется L-тирозин. Если этот процесс нарушается из-за дефицита фермента фенилаланингидроксилазы (КФ 1.14.16.1), то развивается фенилкетонурия.
Полученный из фенилаланина L-тирозин служит предшественником для синтеза дофамина, меланинов, адреналина и норадреналина. В растениях L-фенилаланин является предшественником многих биологически активных веществ, включая лигнин и коричную кислоту.
L-фенилаланин содержится практически во всех белках (за исключением протаминов) — около 7,8% в сывороточном альбумине, 4,6% в гамма-глобулине, 7,7% в овальбумине. Он также входит в состав пептидных гормонов (таких как соматостатин) и опиоидных пептидов (например, энкефалинов), и обнаруживается в организмах в свободной форме. Остатки D-фенилаланина являются компонентом пептидных антибиотиков (например, грамицидина S, полимиксинов, тироцидинов), нейропептидов моллюсков и ракообразных.
d фенилаланин
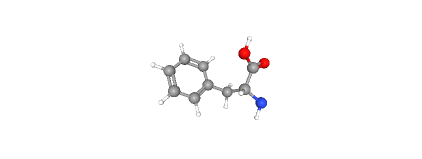
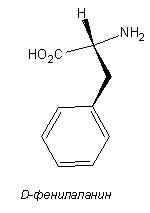
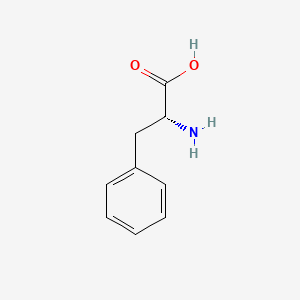 D-фенилаланин выглядит как иглы или призмы.
D-фенилаланин — это D-энантиомер фенилаланина. Это фенилаланин и D-альфа-аминокислота. Это сопряжённое основание D-фенилаланиния. Это сопряжённая кислота D-фенилаланината. Это энантиомер L-фенилаланина. Это таутомер D-фенилаланина.
D-Фенилаланин — это метаболит, который содержится в кишечной палочке (штамм K12, MG1655) или вырабатывается ею.
D-фенилаланин выглядит как иглы или призмы.
D-фенилаланин — это D-энантиомер фенилаланина. Это фенилаланин и D-альфа-аминокислота. Это сопряжённое основание D-фенилаланиния. Это сопряжённая кислота D-фенилаланината. Это энантиомер L-фенилаланина. Это таутомер D-фенилаланина.
D-Фенилаланин — это метаболит, который содержится в кишечной палочке (штамм K12, MG1655) или вырабатывается ею.
Катаболизм фенилаланина
В природе существуют различные пути биологической деградации фенилаланина. Основные промежуточные продукты катаболизма фенилаланина и тесно связанного с ним тирозина у разных организмов включают фумарат, пируват, сукцинат, ацетоацетат, ацетальдегид и другие. У животных и людей фенилаланин и тирозин разлагаются до фумарата (который превращается в оксалоацетат, служащий субстратом для глюконеогенеза) и ацетоацетата (увеличивает содержание кетоновых тел в крови), поэтому эти аминокислоты относятся к глюкокето-гликемическим (смешанным) в зависимости от характера их катаболизма у животных (см. классификацию аминокислот). Основной путь метаболического преобразования фенилаланина у животных и человека заключается в ферментативном гидроксилировании этой аминокислоты, приводящем к образованию другой ароматической аминокислоты — тирозина. Преобразование фенилаланина в тирозин в организме главным образом направлено на устранение излишков фенилаланина, а не на восполнение запасов тирозина, поскольку последний обычно поступает в достаточных количествах вместе с белками пищи, и его дефицит, как правило, не наблюдается. Последующие этапы катаболизма затрагивают уже тирозин. Фенилаланин служит исходным веществом для образования циннамата — одного из ключевых предшественников фенилпропаноидов. Кроме того, фенилаланин способен метаболизироваться в один из биогенных аминов — фенилэтиламин.Нужен ли фенилаланин организму
Аминокислота принимает участие в образовании следующих веществ:- Тирозина, который действует как мощный нейромедиатор;
- Эпинефрина и норэпинефрина, стимулирующих деятельность центральной нервной системы;
- Дофамина, влияющего на настроение, двигательную активность и процесс принятия решений.
Популярные вопросы и ответы
Что такое фенилаланин простыми словами?
Фенилаланин — это незаменимая аминокислота, выполняющая следующие функции:
- умеренное снижение активности энкефалиназ мозга;
- служит важным субстратом для синтеза тирозина, меланина и дофамина;
- участвует в производстве тироксина — гормона щитовидной железы, регулирующего метаболизм;
- стимулирует центральную нервную систему;
- уменьшает зависимость от алкоголя и опиатов;
- повышает болевой порог;
- активизирует функции щитовидной железы.
Чем опасен фенилаланин?
Фенилаланин — это ароматическая альфа-аминокислота, относящаяся к группе незаменимых аминокислот, критически важных для нормального функционирования человеческого организма.
Дефицит фенилаланина может привести к различным неврологическим расстройствам, потере мышечной массы, гормональному дисбалансу, нарушению работы надпочечников и щитовидной железы, а также проблемам с волосами, ногтями и кожей.
Однако избыток фенилаланина тоже опасен: он может вызывать бессонницу, расстройства центральной нервной системы, депрессию, повышенную раздражительность и ухудшение когнитивных функций.
Фенилаланин активно используется в пищевой промышленности для изготовления сахарозаменителей и добавляется в такие продукты, как сладкая газировка, жевательная резинка и кондитерские изделия.
К чему приводит недостаток фенилаланина?
Нехватка фенилаланина может стать причиной нервных расстройств, уменьшения мышечной массы, гормональных нарушений, проблем с работой надпочечников и щитовидной железы, а также выпадения волос и ухудшения состояния кожи и ногтей.
Переизбыток этой аминокислоты также имеет серьезные последствия: он может вызвать проблемы со сном, нарушения в работе центральной нервной системы, депрессию, раздражительность и снижение когнитивных способностей.
Является ли фенилаланин заменимым или нет?
Для взрослого здорового человека незаменимы девять аминокислот: валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан и фенилаланин; иногда к этому списку добавляют гистидин (F V T W M L I K H).
К какой группе относится фенилаланин?
Фенилаланин (Phe или F) — это незаменимая α-аминокислота с химической формулой C9H11NO2. Ее можно представить как бензильное производное аланина, где водородный атом замещен на фенильную группу. Данная аминокислота относится к классу нейтральных и неполярных соединений благодаря своей инертной и гидрофобной бензильной боковой цепи.
Что такое анализ на фенилаланин?
Генетическое исследование мутации гена PAH — это анализ изменений в гене PAH, вызывающих развитие фенилкетонурии.
Фенилаланин — это незаменимая аминокислота, необходимая для синтеза белков и являющаяся предшественником тиреоидных гормонов щитовидной железы, адреналина и меланина.
Мутации в гене PAH вызывают дефект фермента фенилаланин-4-гидроксилазы, что приводит к нарушению обмена веществ: фенилаланин, поступающий с пищей, не перерабатывается, а накапливается в организме.
Какие железы вырабатывают фенилаланин?
Фенилаланин служит строительным элементом для белков и играет ключевую роль в синтезе таких белков, как инсулин, папаин и меланин. Он помогает почкам и печени выводить продукты метаболизма. Этот аминокислотный компонент улучшает секреторную функцию поджелудочной железы и печени.
Кроме того, фенилаланин влияет на работу щитовидной железы и надпочечников, участвуя в образовании тироксина — главного гормона щитовидной железы.
Какая норма фенилаланина в крови?
Нормальный уровень фенилаланина в крови составляет 58 ± 15 мкмоль/л у взрослых, 60 ± 13 мкмоль/л у подростков и 62 ± 18 мкмоль/л у детей. У новорожденных верхняя граница нормы достигает 120 мкмоль/л.